Nieinwazyjne metody diagnostyczne i terapeutyczne zyskują w ostatnich latach coraz większe znaczenie w medycynie weterynaryjnej. Dlatego też w coraz częściej wykorzystuje się biomarkery. Biomarkery to mierzalne związki, które mogą służyć jako wskaźniki różnych procesów fizjologicznych lub patologicznych, a tym samym mają znaczenie prognostyczne lub diagnostyczne. W niektórych przypadkach biomarkery mogą dostarczyć ważnych dodatkowych informacji do uzyskania pełnego obrazu klinicznego, a tym samym wpływać na decyzje medyczne. Biomarkery molekularne można oznaczać w próbkach biologicznych (takich jak surowica, osocze lub płyn mózgowo-rdzeniowy) i mogą to być specyficzne cząsteczki, enzymy lub hormony.
Szczególnie w diagnostyce nowotworów biomarkery stanowią pomocne i nieinwazyjne narzędzia diagnostyki, prognozowania i monitorowania leczenia. W medycynie koni diagnostyka nowotworów nabiera coraz większego znaczenia ze względu na starzenie się populacji tych zwierząt i nadal stanowi wyzwanie dla lekarza ze względu na ograniczone zastosowanie technik obrazowania u koni (klatka piersiowa, brzuch). Co więcej, u koniowatych cierpiących na choroby nowotworowe występują raczej niespecyficzne objawy, takie jak gorączka, wyniszczenie lub lekka anemia, liczba białych krwinek często zmienia się tylko nieznacznie, a zespoły paranowotworowe (takie jak hiperkalcemia) występują rzadko.
Może to znacznie utrudnić rozpoznanie. Chłoniak koński (mięsak limfatyczny) jest najczęstszą złośliwą chorobą nowotworową koni i może objawiać się w postaci jelitowej, skórnej, śródpiersiowej lub wieloośrodkowej (Ryc. 1). W zależności od stadium choroby i umiejscowienia guza pobieranie próbek do diagnostyki histopatologicznej jest często niemożliwe.
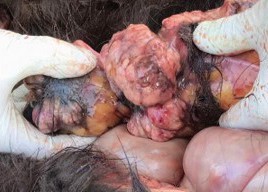
Ryc. 1: Wyniki sekcji zwłok 3-letniej klaczy islandzkiej. Koń miał gorączkę, krwawienie z nosa i pogorszony stan ogólny. Diagnostyka laboratoryjna wykazała ciężką anemię (erytrocyty 1,55 T/l, hematokryt 0,08 l/l, hemoglobina 54 g/l) z trombocytopenią (17 G/l). W badaniu histopatologicznym stwierdzono chłoniaka.
Ostatnio zaczęto wykorzystywać kinazę tymidynową jako marker proliferacji w diagnostyce nowotworów koni. Kinaza tymidynowa jest enzymem komórkowym, który odgrywa decydującą rolę podczas syntezy DNA, kiedy nukleozyd – tymidyna – jest włączany do DNA, dlatego jej stężenie w surowicy koreluje dodatnio z szybkością podziału komórek. Ponieważ złośliwe choroby układu krwiotwórczego i chłonnego (chłoniak, białaczka, szpiczak mnogi) wiążą się często z silną proliferacją, kinazę tymidynową można określić jako tzw. marker proliferacji. Ciężkie zapalenie może także prowadzić do niewielkiego wzrostu kinazy tymidynowej, zatem należy je wziąć pod uwagę w diagnostyce różnicowej. W takim przypadku należy dodatkowo oznaczyć białka ostrej fazy. Ujemny wynik nie wyklucza choroby nowotworowej.
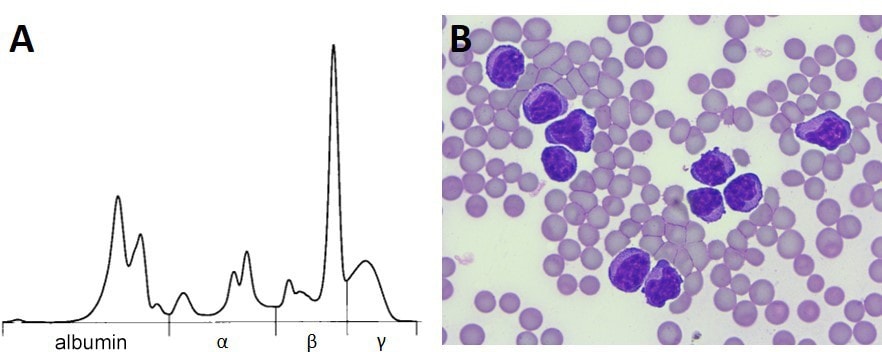
Ryc. 2: Krzywa elektroforezy białek surowicy z monoklonalnym pikiem we frakcji beta (A). Koń wykazywał ciężką leukocytozę, w tym liczne atypowe limfocyty we krwi obwodowej (B), znacznie podwyższone stężenie amyloidu A w surowicy (850,15 μg/ml) i poziom kinazy tymidynowej w surowicy wynoszący 19,3 U/l (norma <3 U/l).
Elektroforeza białek surowicy może być dodatkową opcją diagnostyczną – do tego bardzo ekonomiczną – w przypadku podejrzenia nowotworu. Zmiany monoklonalne, często we frakcji beta lub gamma, są wynikiem nadmiernej produkcji specyficznej immunoglobuliny przez klon komórek plazmatycznych i zostały opisane głównie w chorobach limfoproliferacyjnych (Ryc. 2 A i B).
Jeśli podejrzewa się nowotwór wątroby (np. raka wątrobowokomórkowego), można oznaczyć alfa-1-fetoproteinę (AFP). AFP jest glikoproteiną, która jest fizjologicznie wytwarzana u źrebiąt do 1,5 roku życia, jej poziom jest więc też podwyższony również u ciężarnych klaczy. U koni dorosłych i nieźrebnych klaczy wzrost może wskazywać na nowotwór wątroby, ponieważ AFP jest wytwarzana przez komórki nowotworowe wątroby, co skutkuje jej podwyższonym stężeniem w surowicy. Fosfataza alkaliczna (AP) jest rzadziej stosowana w diagnostyce nowotworów wątroby. Zwiększona aktywność enzymatyczna AP w surowicy jest bardziej prawdopodobna przy nowotworach kości (np. kostniakomięsaku), chociaż występują one raczej rzadko u koni.
Dość powszechnym typem nowotworu u klaczy jest ziarniszczak (GCT). Rozpoznanie często można jednoznacznie postawić, oznaczając hormon antymüllerowski (AMH). AMH jest glikoproteiną, która wpływa na różnicowanie płciowe podczas rozwoju embrionalnego i jest wytwarzana przez komórki ziarniste podczas folikulogenezy u dojrzałych samic oraz przez komórki Sertolego w tkance jąder u samców. Dzięki temu hormon AMH może być stosowany jako marker diagnostyczny nie tylko w diagnostyce nowotworów, lecz także w wielu innych kwestiach klinicznych.
AMH jest najbardziej czułym markerem diagnostycznym (98%) w diagnostyce ziarniszczaków w porównaniu z inhibiną (80-90%) i testosteronem (50%). Zazwyczaj klacze wykazują kliniczne objawy okresu bezrujowego, bardzo niski poziom progesteronu (<1 ng/ml) i jednostronnie powiększony jajnik, w badaniu ultrasonograficznym wyglądem przypominający plaster miodu. Drugi jajnik z kolei jest zwykle znacznie mniejszy. Często odróżnienie go od innych schorzeń jajników, np. krwiaka, potworniaka czy torbielakogruczolaka, na podstawie USG nie jest możliwe. Pomocne może być tutaj oznaczenie AMH, ponieważ jest on wytwarzany w dużych ilościach przez komórki ziarniste. Jeśli oznaczenie AMH nie daje miarodajnego wyniku (np. gdy ziarniszczak dopiero zaczyna się rozwijać), zaleca się ponowne badanie najwcześniej po 3-4 miesiącach. Ponadto rozpoznanie GCT na podstawie oznaczenia AMH jest również możliwe w czasie ciąży, ponieważ poziom AMH w surowicy, w przeciwieństwie do testosteronu czy inhibiny, nie zmienia się w zaawansowanej ciąży.
Również w normalnym cyklu klaczy AMH nie podlega znaczącym wahaniom i – w przeciwieństwie do testosteronu (kora nadnerczy) – jest wytwarzany jedynie w jajniku. U starszych (> 20 lat) klaczy może wystąpić spadek poziomu AMH korelujący ze zmniejszeniem rezerwy pęcherzykowej (pęcherzyki pierwotne).
Oznaczanie AMH może być również przydatne u ogierów. W przeciwieństwie do siarczanu estronu, stężenie AMH u samców ma decydujące znaczenie dla rozpoznania wnętrostwa niezależnie od wieku, a zatem stanowi użyteczny biomarker obecności tkanki jąder. Podstawowy poziom testosteronu u ogierów z wnętrostwem może być niski lub graniczny i dostarcza niewiele informacji, gdy zostanie oznaczony jako jedyny parametr. Dlatego testosteron należy zawsze mierzyć podczas wykonywania testu stymulacji hCG (wartość podstawowa i wartość po stymulacji). Ze względu na dość długi okres półtrwania (1,5 – 2 dni), AMH należy oznaczyć dopiero po minimum 2 tygodniach od kastracji, ponieważ wówczas stężenie w surowicy zmniejszy się do poziomu rozstrzygającego diagnostycznie. Przed upływem tych 14 dni odpowiedniejszy będzie testosteron, ponieważ ma znacznie krótszy okres półtrwania (ok. 1 h). Bardzo niski poziom AMH u ogierów zdrowych może świadczyć o zwyrodnieniu jąder lub wiązać się z porą roku (jesień / zima). Zwyrodnienie jąder związane z wiekiem występuje częściej u ogierów w podeszłym wieku, ale sam poziom AMH nie dostarcza informacji na temat płodności zwierzęcia. Z drugiej strony bardzo wysoki poziom w połączeniu z objawami klinicznymi może wskazywać na guza z komórek Sertolego i zawsze należy to sprawdzić za pomocą badania histopatologicznego.
Biomarkery odgrywają rolę nie tylko w diagnostyce onkologicznej. Jeśli podejrzewa się stan zapalny, białka ostrej fazy, takie jak surowiczy amyloid A (SAA) lub fibrynogen, mogą być również pomocne w ocenie klinicznie niewidocznego nasilenia zapalenia lub w ocenie skuteczności terapeutycznej.
Ogólnie białka ostrej fazy dzielą się na ujemne, których stężenie we krwi spada podczas odpowiedzi ostrej fazy (np. albuminy), oraz dodatnie, których stężenie z kolei wzrasta w czasie zapalenia. Dodatnie białka ostrej fazy mają duży (szybki, 10- do 1000-krotny wzrost w krótkim czasie), umiarkowany (powolny wzrost, 5- do 10-krotny z fazą plateau) lub niski poziom wzrostu stężenia (0,5 do 5-krotny).
Produkcja białek ostrej fazy jest inicjowana podczas ostrej fazy odczynu zapalnego. Jest to wczesna, niespecyficzna reakcja ogólnoustrojowa na uszkodzenie tkanki w wyniku zakażenia (bakteryjnego, wirusowego lub inwazji pasożytniczej), urazu lub nowotworu. Oprócz działania miejscowego i ogólnoustrojowego, uwalnianie mediatorów odpowiedzi zapalnej, takich jak cytokiny prozapalne, stymuluje ona syntezę białek ostrej fazy w hepatocytach wątroby.
U koni oznaczanie SAA jako głównego białka ostrej fazy jest coraz częściej stosowane w klinicznej diagnostyce laboratoryjnej. SAA jest apolipoproteiną, która z jednej strony chemotaktycznie rekrutuje komórki zapalne do obszaru objętego stanem zapalnym, a z drugiej – hamuje proliferację limfocytów. U zdrowych koni SAA w surowicy można wykryć tylko w bardzo niskich stężeniach. Jeśli obecny jest szkodliwy czynnik, następuje bardzo szybki (w ciągu 6-12 godzin) i silny wzrost stężenia (od 100 do 1000 razy), a także bardzo szybki jego spadek po usunięciu szkodliwego czynnika (w ciągu 12 godzin). SAA jest bardzo czułym markerem wczesnych procesów zapalnych, który może stanowić ważną pomoc w diagnostyce, rokowaniu i monitorowaniu. Zwłaszcza gdy niezbędne jest szybkie działanie, jak na przykład w medycynie źrebiąt, poziomy SAA można mierzyć w celu wykrycia posocznicy, bakteryjnego zapalenia płuc lub septycznego zapalenia stawów we wczesnym stadium. Poziomy SAA w surowicy mogą również pomóc w odróżnieniu zakażeń bakteryjnych i wirusowych, ale zawsze należy je interpretować w kontekście ogólnego badania klinicznego i innych parametrów laboratoryjnych, ponieważ SAA jest nieswoistym białkiem ostrej fazy. Nieznacznie podwyższony poziom może wystąpić w wyniku stresu, transportu, szczepień lub po ciężkim wysiłku. Ponadto podwyższony SAA nigdy nie powinien być jedynym kryterium wdrożenia antybiotykoterapii. Należy również uwzględnić liczbę białych krwinek, chemię kliniczną i inne markery zapalenia oraz oczywiście badania kliniczne i bakteriologiczne.
Fibrynogen, to białko ostrej fazy o umiarkowanym poziomie wzrostu stężenia, również jest stosowany jako narzędzie diagnostyczne w medycynie koni. W porównaniu z SAA wzrasta tylko 1- do 2-krotnie w ciągu pierwszych 24 godzin od zadziałania szkodliwego czynnika i osiąga maksimum po upływie ok. 48 godzin. Fibrynogen może się utrzymywać na wysokim poziomie przez kilka tygodni i dlatego nie jest tak czuły podczas monitorowania. Fibrynogen można oznaczyć jedynie z osocza cytrynianowego.
Szybkie i wczesne rozpoznanie ma znaczenie nie tylko w ostrym zapaleniu, lecz także w odniesieniu do narządów o niskim współczynniku regeneracji, takich jak mięsień sercowy. Przydatnym biomarkerem ostrej martwicy mięśnia sercowego jest troponina I, którą można stosować jako specyficzny parametr kardiologiczny u koni. Troponiny sercowe to białka, które odgrywają rolę w regulacji skurczu i rozluźnienia mięśnia sercowego. Jeśli komórki są uszkodzone, zwiększone stężenie troponiny sercowej w surowicy można wykryć po ok. 5-7 godzinach. Przyczyną mogą być: choroby wirusowe lub bakteryjne, wrodzone choroby serca, niedobory, toksyny lub nowotwory.
Podsumowując, w klinicznej diagnostyce laboratoryjnej dostępnych jest kilka różnych, bardzo czułych biomarkerów. Oddzielnie lub łącznie mogą zapewnić odpowiednią pomoc w praktyce weterynaryjnej w zakresie rozpoznania, oceny rokowania i przewidywania sukcesu terapeutycznego, a także wspomagania decyzji o doborze leczenia.

Svenja Möller



