Reakcja ostrej fazy (ang. acute-phase response APR) to wczesna reakcja ogólnoustrojowa na bodźce zapalne, infekcje i uszkodzenia tkanek. Powstawanie specyficznych białek ostrej fazy (ang. acute-phase proteins APP) w wątrobie jest regulowane przez cytokiny prozapalne (IL-6, IL-1β, TNF-α), których stężenie we krwi rośnie lub spada podczas APR. APP są cennymi markerami do wykrywania i monitorowania postępu procesów zapalnych, a także chorób nowotworowych. APR występuje znacznie wcześniej i bardziej swoiście niż zmiana liczby leukocytów.
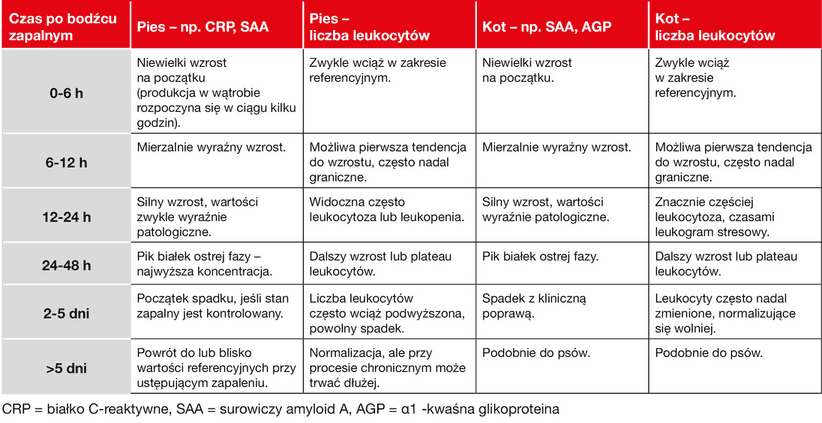
APP klasyfikuje się ze względu na siłę odpowiedzi: silnie reagujące (wzrost 10–100-krotny), umiarkowanie reagujące (wzrost 2–10-krotny) i słabo reagujące (wzrost <2-krotny). Pomiar stężenia dużych APP jest szczególnie przydatny do wczesnej diagnostyki i monitorowania chorób związanych z APR. U psów głównym APP jest białko C-reaktywne (CRP), natomiast u kotów dominuje surowiczy amyloid A (SAA). Haptoglobina (Hp) i α1-kwaśna glikoproteina (AGP) są uważane za APP reagujące umiarkowanie lub nieznacznie. Albumina, transferyna i paraoksonaza to ujemne APP, których stężenia zazwyczaj spadają podczas reakcji ostrej fazy. Zachowanie poszczególnych APP podczas APR podsumowano w Tabeli 1.
Psy – CRP jako złoty standard
Białko C-reaktywne (CRP), jako główne białko ostrej fazy, wzrasta w ciągu 4–24 godzin od wystąpienia czynnika wyzwalającego, wzrastając nawet 50–100-krotnie, osiągając szczyt po 1–2 dniach i szybko spadając w miarę skutecznej terapii. Ze względu na tę dynamiczną charakterystykę, CRP jest szczególnie przydatne do wczesnego wykrywania, monitorowania postępu choroby i oceny skuteczności terapii.
Podwyższony poziom CRP obserwuje się w szeregu procesów zapalnych i immunologicznych, w tym w zakażeniach bakteryjnych, chorobach pasożytniczych, chorobach autoimmunologicznych, nowotworach oraz zmianach pourazowych lub pooperacyjnych. U psów z ostrą infekcją Babesia canis, poziom CRP wykazuje silną korelację z ciężkością objawów klinicznych i parametrami hematologicznymi.
W ramach kontroli i oceny antybiotykoterapii wykazano, że antybiotyki można odstawić po zaobserwowaniu poprawy klinicznej i powrocie stężenia CRP do normy, co znacznie skraca czas leczenia wielu chorób.
W grzybicach układowych, takich jak kokcydioidomykoza płucna, CRP w połączeniu z haptoglobiną (Hp) również wykazało wartość predykcyjną remisji. Jednak poziom CRP może być podwyższony przy braku stanu zapalnego, na przykład podczas ekstremalnego wysiłku fizycznego lub w ciąży, dlatego jego interpretacja musi zawsze uwzględniać kontekst kliniczny.
Wskaźnik ostrej fazy (API) – marker łączony
Najnowsze badania połączyły dodatnie APP (CRP, Hp) i ujemne APP (albumina, opcjonalnie PON-1) w indeks ostrej fazy (API). Wskaźnik ten odzwierciedla ogólną aktywność stanu zapalnego. Psy z nowotworami złośliwymi i wysokim API miały znacznie gorsze rokowanie.
W przewlekłych chorobach zapalnych, takich jak leiszmanioza u psów, poziom CRP i Hp utrzymuje się stale na podwyższonym poziomie, podczas gdy poziom albuminy i transferyny często spada. Zmiany w API ściśle korelują z odpowiedzią na leczenie i aktywnością choroby. Utrzymujące się wysokie wartości wskazują na resztkową aktywność, koinfekcje lub niepowodzenie leczenia.
Koty – uwaga na SAA i AGP
U kotów dynamika i znaczenie APP znacznie różnią się od tych u psów. Najważniejszym APP jest surowiczy amyloid A (SAA), natomiast α1-kwaśna glikoproteina (AGP) ma szczególne znaczenie diagnostyczne w zakaźnym zapaleniu otrzewnej kotów (FIP).
Surowiczy amyloid A (SAA)
SAA jest białkiem bardzo czułym, reaguje bardzo wcześnie, szybko osiągając wysokie stężenia, co czyni go odpowiednim zarówno do wczesnej diagnostyki, jak i oceny prognostycznej. Szybki spadek stężenia wskazuje na dobrą odpowiedź na leczenie, natomiast stagnacja sugeruje utrzymujący się stan zapalny lub infekcję wtórną. Nowoczesne testy turbidymetryczne z wykorzystaniem przeciwciał monoklonalnych zapewniają wysoką precyzję diagnostyczną. Dalsze badania wykazują przydatność SAA, zwłaszcza w zakażeniach bakteryjnych, takich jak odmiedniczkowe zapalenie nerek.
Alfa-1 kwaśna glikoproteina (AGP)
AGP to umiarkowanie rosnące białko ostrej fazy o dużym znaczeniu klinicznym dla FIP. Podwyższone stężenie AGP w surowicy potwierdza wstępne rozpoznanie, gdy jest interpretowane łącznie z innymi wynikami. W szczególności, podczas terapii przeciwwirusowej stężenie AGP wykazuje dynamiczne zmiany.
Haptoglobina (Hp)
Zarówno u psów, jak i u kotów Hp jest umiarkowanym białkiem ostrej fazy syntetyzowanym w wątrobie. Jego główną funkcją biologiczną jest wiązanie z wysokim powinowactwem wolnej hemoglobiny (Hb) z lizowanych erytrocytów, co zmniejsza oksydacyjne uszkodzenia tkanek i zapobiega utracie żelaza związanego z Hb. Podczas ostrych procesów zapalnych u obu gatunków obserwuje się mniej wyraźny i opóźniony wzrost stężenia Hp w porównaniu z głównymi białkami ostrej fazy, takimi jak SAA czy CRP. Podobnie jak u innych ssaków, hemoliza wewnątrznaczyniowa może prowadzić do spadku stężenia haptoglobiny, ponieważ białko to jest szybko zużywane poprzez wiązanie dużych ilości wolnej hemoglobiny.
Negatywne białka ostrej fazy
Albuminy
Stężenie albumin spada z powodu redystrybucji aminokwasów do syntezy dodatnich APP oraz zwiększonej przepuszczalności naczyń włosowatych. Jest to cenny wskaźnik stanu zapalnego o charakterze ogólnoustrojowym, ale należy go interpretować w kontekście stanu nawodnienia, utraty białka i funkcji wątroby. U psów albuminy są uwzględniane w obliczaniu wskaźnika ostrej fazy (API).
Transferyna
Transferyna, białko transportujące wiążące żelazo, zmniejsza się w reakcji ostrej fazy, zmniejszając dostępność żelaza dla mikroorganizmów. U psów zaobserwowano znaczny spadek transferyny podczas infekcji bakteryjnych. U kotów odnotowano również znaczny spadek w przypadkach przewlekłego stanu zapalnego.
Białka ostrej fazy w FIP
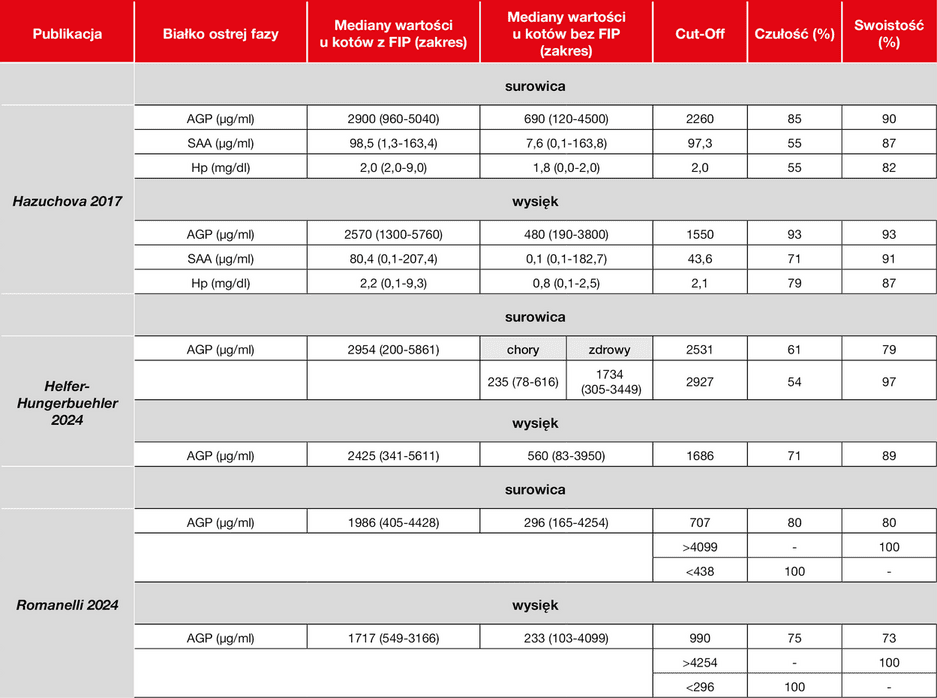
Zakaźne zapalenie otrzewnej kotów (FIP) to choroba zapalna, która zazwyczaj wiąże się ze wzrostem stężenia białek ostrej fazy. Badania wykazały, że pomiar stężenia AGP w wysiękach jest najbardziej miarodajną metodą różnicowania kotów z i bez FIP. Zdefiniowano różne zakresy wartości cut-off o zróżnicowanej czułości i swoistości (Tabela 2). Niektóre z tych zakresów, na przykład w pracy Helfer Hungerbühler i in. (AGP > 2927), charakteryzują się wysoką swoistością (97%) i dlatego mogą silnie wskazywać na FIP. Jednak ze względu na stosunkowo niską czułość (54%), prawie połowa kotów z FIP może zostać nie wykryta. Należy również zauważyć, że APP mogą wzrastać w innych chorobach. Koty z septycznym zapaleniem otrzewnej lub rozsianymi nowotworami często wykazują stężenia AGP podobne do obserwowanych u kotów z FIP. Dlatego uzupełniające badania cytologiczne i bakteriologiczne są ważne, aby wykluczyć rozpoznanie różnicowe.
Samo oznaczenie AGP jest niewystarczające do postawienia ostatecznej diagnozy i powinno być traktowane jako jeden z wielu elementów procesu diagnostycznego. AGP może również odgrywać ważną rolę w monitorowaniu terapii u kotów z FIP. Podczas leczenia AGP stopniowo spada, chociaż wolniej niż SAA. Jest to prawdopodobnie spowodowane dłuższym okresem półtrwania AGP, co oznacza, że stężenia AGP w 2. dniu terapii FIP mogą być wyższe niż przed rozpoczęciem leczenia. Znaczący spadek AGP obserwowano od 7. dnia po rozpoczęciu terapii. Do 28. dnia poziom AGP mieścił się w zakresie normy u prawie wszystkich kotów (Helfer-Hungerbuehler 2024: 17 z 18 kotów, Zuzzi-Krebitz 2024: 37 z 39 kotów), co czyni go wiarygodnym parametrem monitorowania skuteczności leczenia. Natomiast stężenie SAA znacząco spadło już 2. dnia, a u większości kotów osiągnęło (prawie) prawidłowe stężenie w ciągu 4–7 dni. Addie i współpracownicy (2022) wykorzystują AGP jako marker różnicujący remisję od wyzdrowienia.
Wyzdrowienie oznacza całkowite wyleczenie z FIP, natomiast remisję definiuje się jako etap pośredni między wyzdrowieniem a śmiercią, wciąż niosący ze sobą ryzyko nawrotu. U kotów, które w pełni wyzdrowiały, stężenia AGP mieściły się w normie, natomiast u kotów w remisji obserwowano podwyższone stężenie AGP. Dlatego wzrost stężenia AGP może również wskazywać na potencjalny nawrót FIP.
Dr. Ruth Klein, Katharina Buchta
Literatura uzupełniająca:
Malin K, Witkowska-Piłaszewicz O. C-Reactive Protein as a Diagnostic Marker in Dogs: A Review. Animals (Basel). 2022 Oct 21;12(20):2888. doi: 10.3390/ani12202888.
von Hohnhorst IM, Moritz A, Eisenecker CM, Strube C, Rodjana KE, Müller E, Schäfer I. Impact of levels of parasitemia and antibodies, acute-phase proteins, as well as stays abroad on hematological and biochemical parameters in 342 dogs with acute Babesia canis infection. Parasit Vectors. 2025 Aug 15;18(1):347. doi: 10.1186/s13071-025-06997-4.
Glick A, Jaffey JA, Kreisler R, Hanzlicek AS, Ringold R. Serum C-reactive protein and haptoglobin decrease in the first three months of treatment and relative change in haptoglobin predict remission in dogs with pulmonary coccidioidomycosis. J Am Vet Med Assoc. 2024 Jun 19;262(9):1222-1230. doi: 10.2460/javma.24.05.0296.
Baldin M, Gelain ME, Marolato G, Bedin S, Berlanda M, Zanetti M, Torrigiani F, Giordano A, Moretti P, Scavone D, Bonsembiante F. Beyond Individual Acute Phase Protein Assessments: Introducing the Acute Phase Index (API) as a Prognostic Indicator in Dogs with Malignant Neoplasia. Vet Sci. 2025 Jun 1;12(6):533. doi: 10.3390/vetsci12060533.
Fernandes Rodrigues N, Giraud L, Bolen G, Fastrès A, Clercx C, Gommeren K, Billen F. Antimicrobial discontinuation in dogs with acute aspiration pneumonia based on clinical improvement and normalization of C-reactive protein concentration. J Vet Intern Med. 2022 May;36(3):1082-1088. doi: 10.1111/jvim.16405.
Viitanen SJ, Lappalainen AK, Christensen MB, Sankari S, Rajamäki MM. The Utility of Acute-Phase Proteins in the Assessment of Treatment Response in Dogs With Bacterial Pneumonia. J Vet Intern Med. 2017 Jan;31(1):124-133. doi: 10.1111/jvim.14631.
Yuki M, Inden T, Hirano T, Naito E, Taira H, Yokota S, Narita M. Comparison of polyclonal and monoclonal antibody assays for serum amyloid A in cats: a study based on an automated turbidimetric immunoassay in a primary care veterinary hospital. Am J Vet Res. 2024 Jul 12;85(9):ajvr.24.03.0067. doi: 10.2460/ajvr.24.03.0067.
Waugh EM, Haining H, Harvie J, Ridyard AE, Eckersall PD. Validation of an automated immunoturbidimetric assay for feline serum amyloid A. BMC Vet Res. 2022 Sep 28;18(1):359. doi: 10.1186/s12917-022-03456-5.
Kurtz M, Pey PBM, Mortier J, Manassero M, Da Riz F, Canonne-Guibert M, Maurey C, Benchekroun G. Usefulness of serum amyloid A for the diagnosis of pyelonephritis in cats: A prospective evaluation. J Vet Intern Med. 2024 May-Jun;38(3):1542-1552. doi: 10.1111/jvim.17082.
Helfer-Hungerbuehler AK, Spiri AM, Meili T, Riond B, Krentz D, Zwicklbauer K, Buchta K, Zuzzi-Krebitz AM, Hartmann K, Hofmann-Lehmann R, Meli ML. Alpha-1-Acid Glycoprotein Quantification via Spatial Proximity Analyte Reagent Capture Luminescence Assay: Application as Diagnostic and Prognostic Marker in Serum and Effusions of Cats with Feline Infectious Peritonitis Undergoing GS-441524 Therapy. Viruses.
2024 May 16;16(5):791. doi: 10.3390/v16050791.
Tršar L, Štrljič M, Svete AN, Koprivec S, Tozon N, Žel MK, Pavlin D. Evaluation of selected inflammatory markers in cats with feline infectious peritonitis before and after therapy. BMC Vet Res. 2025 May 9;21(1):330. doi: 10.1186/s12917-025-04731-x.
Ceron JJ, Pardo-Marin L, Caldin M, Furlanello T, Solano-Gallego L, Tecles F, Bernal L, Baneth G, Martinez-Subiela S. Use of acute phase proteins for the clinical assessment and management of canine leishmaniosis: general recommendations. BMC Vet Res. 2018 Jun 20;14(1):196. doi: 10.1186/s12917-018-1524-y.
Rossi G. Acute phase proteins in cats: Diagnostic and prognostic role, future directions, and analytical challenges. Vet Clin Pathol. 2023 Feb;52 Suppl 1:37-49. doi: 10.1111/vcp.13238.
Martínez-Subiela S, Ceron JJ. Evaluation of acute phase protein indexes in dogs with leishmaniasis at diagnosis, during and after short-term treatment. Vet Med – Czech, 2005, 50(1):39-46. doi: 10.17221/5595-VETMED.
Paltrinieri S. The feline acute phase reaction. Vet J. 2008 Jul;177(1):26-35. doi: 10.1016/j.tvjl.2007.06.005.
Eckersall PD, Bell R. Acute phase proteins: Biomarkers of infection and inflammation in veterinary medicine. Vet J. 2010 Jul;185(1):23-7. doi: 10.1016/j.tvjl.2010.04.009.
Ceron JJ, Eckersall PD, Martýnez-Subiela S. Acute phase proteins in dogs and cats: current knowledge and future perspectives. Vet Clin Pathol. 2005 Jun;34(2):85-99. doi: 10.1111/j.1939-165x.2005.tb00019.x.
Shih AW, McFarlane A, Verhovsek M. Haptoglobin testing in hemolysis: measurement and interpretation. Am J Hematol. 2014 Apr;89(4):443-7. doi: 10.1002/ajh.23623.
Hazuchova K, Held S, Neiger R. Usefulness of acute phase proteins in differentiating between feline infectious peritonitis and other diseases in cats with body cavity effusions. J Feline Med Surg. 2017 Aug;19(8):809-816. doi: 10.1177/1098612X16658925.
Tasker S, Addie DD, Egberink H, Hofmann-Lehmann R, Hosie MJ, Truyen U, Belák S, Boucraut-Baralon C, Frymus T, Lloret A, Marsilio F, Pennisi MG, Thiry E, Möstl K, Hartmann K. Feline Infectious Peritonitis: European Advisory Board on Cat Diseases Guidelines. Viruses. 2023 Aug 31;15(9):1847. doi: 10.3390/v15091847.
Zuzzi-Krebitz AM, Buchta K, Bergmann M, Krentz D, Zwicklbauer K, Dorsch R, Wess G, Fischer A, Matiasek K, Hönl A, Fiedler S, Kolberg L, Hofmann-Lehmann R, Meli ML, Spiri AM, Helfer-Hungerbuehler AK, Felten S, Zablotski Y, Alberer M, Both UV, Hartmann K. Short Treatment of 42 Days with Oral GS-441524 Results in Equal Efficacy as the Recommended 84-Day Treatment in Cats Suffering from Feline Infectious Peritonitis with Effusion-A Prospective Randomized Controlled Study. Viruses. 2024 Jul 16;16(7):1144. doi: 10.3390/v16071144.
Addie DD, Silveira C, Aston C, Brauckmann P, Covell-Ritchie J, Felstead C, Fosbery M, Gibbins C, Macaulay K, McMurrough J, Pattison E, Robertson E. Alpha-1 Acid Glycoprotein Reduction Differentiated Recovery from Remission in a Small Cohort of Cats Treated for Feline Infectious Peritonitis. Viruses. 2022 Apr 1;14(4):744. doi: 10.3390/v14040744.
Romanelli P, Bertazzolo W, Prisciandaro A, Leone A, Bonfanti U, Paltrinieri S. Measurement of Feline Alpha-1 Acid Glycoprotein in Serum and Effusion Using an ELISA Method: Analytical Validation and Diagnostic Role for Feline Infectious Peritonitis. Pathogens. 2024 Mar 29;13(4):289. doi: 10.3390/pathogens13040289.


